Chemická vazba
13. 7. 2021 2021-08-04 13:57Chemická vazba
Chemická vazba
CHEMICKÁ VAZBA
Molekula a chemická sloučenina
Atomy téměř všech chemických prvků se spojují do větších částic – molekul nebo
krystalů.
Molekula je částice chemické látky, složená ze dvou nebo více sloučených atomů.
Sloučenina je chemická látka, složená ze sloučených atomů dvou nebo více prvků.
Většina látek se skládá z atomů, které jsou vzájemně spojeny chemickou vazbou.
Chemická vazba
Chemická vazba jsou soudržné síly mezi atomy v molekulách a v krystalech.
Při slučování atomů prvků se na vzniku chemické vazby podílejí valenční
elektrony.
Chemická vazba vzniká tak, že val. elektron atomu vytvoří s val. elektronem
dalšího atomu společný elektronový pár.
Valenční elektron označujeme u značky prvku tečkou a vazbu označujeme čárkou mezi
značkami.
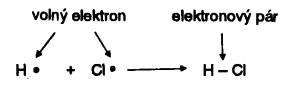
Vznik chemické vazby v chlorovodíku
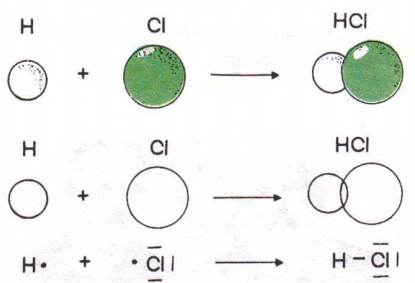
Vznik chemické vazby
Chemická vazba mezi dvěma atomy vzniká utvořením vazebného elektronového
páru. Ten většinou oba atomy společně sdílejí.
Každý z atomů se však snaží přitáhnout vazebný elektronový pár ke svému
atomovému jádru. Síla atomu, kterou se snaží přitáhnout elektronový pár, se
nazývá elektronegativita atomu.
Značí se X a je uváděna v periodické tabulce prvků. Čím je její hodnota vyšší, tím
více atom přitahuje elektronový pár ke svému jádru.
Např. elektronegativita atomů chloru X(Cl) = 2,8, atomů vodíku X(H) = 2,1.
Elektronegativita (X)
= schopnost atomů přitáhnout vazebný elektronový pár.
Podle rozdíku hodnot elektronegativit sloučených atomů rozlišujeme několik typů
chemické vazby.
Typy chemické vazby
• nepolární – mezi stejnými atomy nebo s rozdílem elektronegativit < 0,4
(nebo X< 0,4)
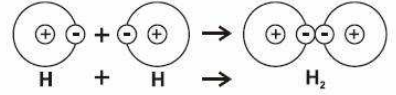
• polární – rozdíl elektronegativit atomů > 0,4 a zároveň < 1,7
(nebo 0,4 < X <1,7)
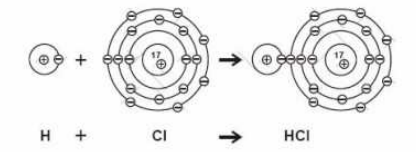
• iontová – rozdíl elektronegativit atomů > 1,7
(nebo X > 1,7). Její podstatou jsou přitažlivé síly mezi kationty a anionty.
Dochází k odtržení val. elektronu od atomu prvku s nižší elektronegativitou–
elektron přijímá prvek atomu s vyšší elektronegativitou. Vznikají tak ionty.
Např. NaCl – chlorid sodný (kuchyňská sůl)



