Kyselost a zásaditost
15. 7. 2021 2021-08-04 14:03Kyselost a zásaditost
Kyselost a zásaditost
KYSELOST A ZÁSADITOST
Kyselost nebo zásaditost vodných roztoků dovedli lidé určit již velmi dávno.
Rozlišovali roztoky s chutí kyselou (kyselé roztoky) a roztoky s chutí hořkou, louhovitou
(zásadité roztoky).
Používali rovněž látky, které mají jinou barvu v kyselém, neutrálním a zásaditém roztoku.
O výklad kyselého a zásaditého chování látek ve vodném roztoku se pokusil v roce 1887
švédský fyzik Svante Augustus ARRHENIUS (1859-1927).
Jeho představy rozšířili a doplnili později další badatelé.
Zjednodušeně (podle Arrhenia) tedy platí, že:
KYSELOST roztoku způsobují kyseliny, které ve vodném roztoku odštěpují
VODÍKOVÉ KATIONTY H+.
ZÁSADITOST roztoku způsobují hydroxidy, které ve vodném roztoku odštěpují
HYDROXIDOVÉ ANIONTY OH-.
Ve vodě je velice malé množství molekul rozštěpeno na stejný počet kationtů vodíku H+
(přesněji noniových kationtů H3O+) a hydroxidových aniontů OH-:
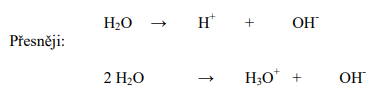
Rozlišujeme 3 typy roztoků:
NEUTRÁLNÍ roztok – pokud koncentrace H+ a OH- zůstává stejná i při rozpuštění nějaké látky ve vodě.
KYSELÝ roztok – jestliže se vodě zvětšuje koncentrace H+ (zvětšuje se i kyselost roztoku).
ZÁSADITÝ roztok – jestliže se ve vodě zvětšuje koncentrace OH- (zvětšuje se i zásaditost roztoku).
Rozlišují se také kyseliny silné, středně silné a slabé, a to podle toho, zda se ve vodě štěpí na
ionty všechny molekuly, část molekul nebo jen velmi málo molekul kyseliny:
• Silné kyseliny – chlorovodíková HCl, sírová H2SO4, dusičná HNO3
• Středně silné – trihydrogenfosforečná H3PO4
• Slabé – uhličitá H2CO3, siřičitá H2SO3
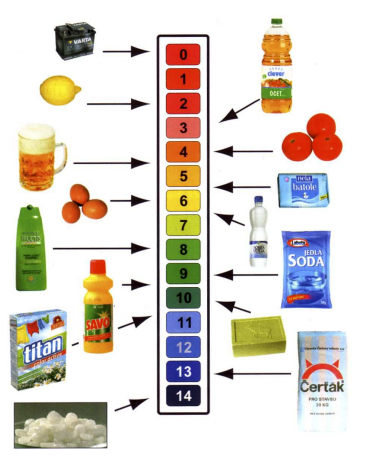
STUPNICE pH
Stupnice pH (čti pé–há) byla zavedena k přesnějšímu určení kyselosti nebo zásaditosti
vodných roztoků.
Je to stupnice od 0 do 14.
V této stupnici má hodnotu:
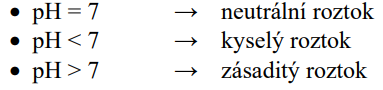
pH je mírou kyselosti kyselin a zásaditosti zásad.
Látky nebo jejich roztoky, které mají pH = 7, označujeme jako NEUTRÁLNÍ.
Látky nebo jejich roztoky, které mají pH < 7, označujeme jako KYSELÉ.
Látky nebo jejich roztoky, které mají pH > 7, označujeme jako ZÁSADITÉ.
V domácnosti často provádíme např. měření pH vody v bazénech. Vyšší hodnoty pH omezují
tvorbu řas ve vodě.
Jistě jste už slyšeli také o žvýkačkách, které upravují pH v ústech.
INDIKÁTORY
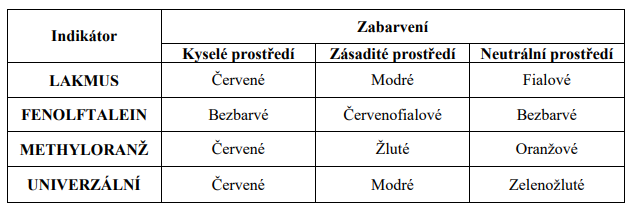
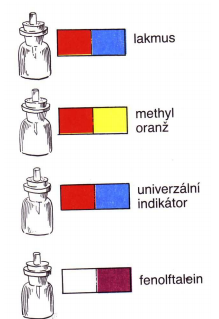
Indikátory jsou látky, které při změně kyselosti nebo zásaditosti roztoku MĚNÍ BARVU
(v závislosti na hodnotě pH roztoku).
Hodnoty pH roztoku se přibližně určují podle barvy univerzálních indikátorů a přesně měří
přístroji pH – metry.

Přehled nejčastěji používaných indikátorů: